Технологии искусственного интеллекта в здравоохранении
Информационные сервисы и искусственный интеллект в помощь врачу — анестезиологу-реаниматологу
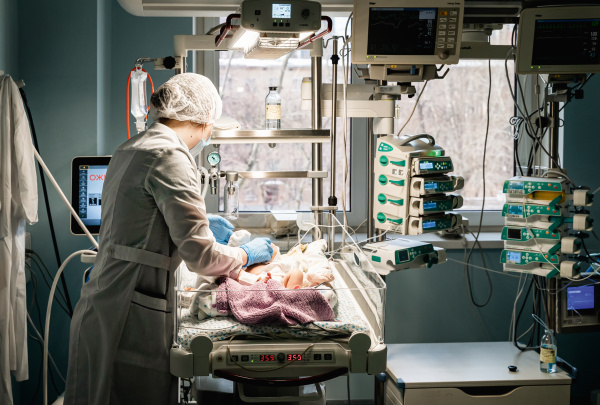
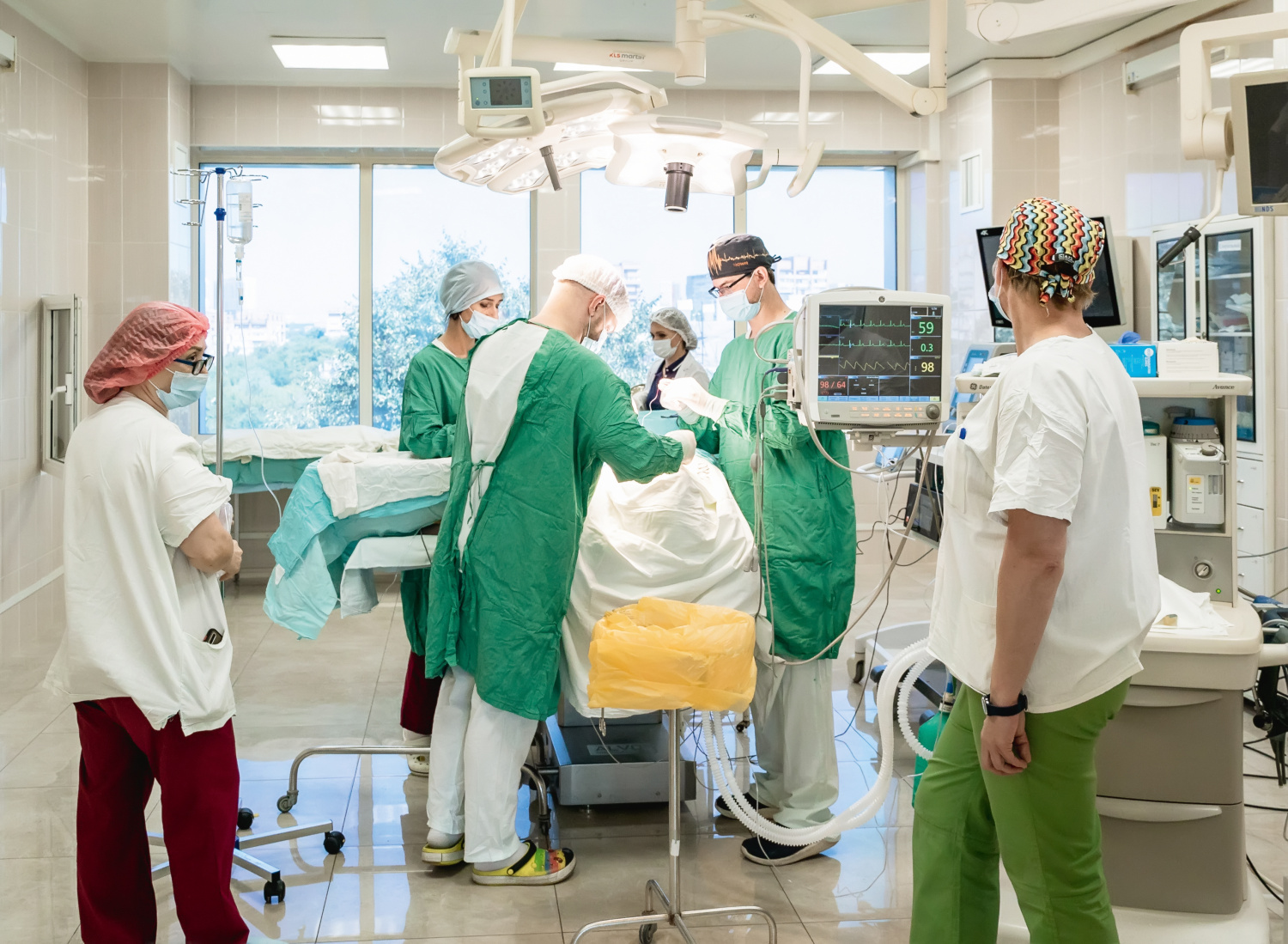
В отделениях анестезиологии и реанимации, интенсивной терапии и экстренной помощи персонал, особенно врачи, работают в условиях большой информационной нагрузки. Ургентная помощь сама по себе требует быстрого принятия решений и отлаженных действий. Поддержать медицинских сотрудников способны информационные сервисы, в том числе с искусственным интеллектом.Технологии искусственного интеллекта в здравоохранении
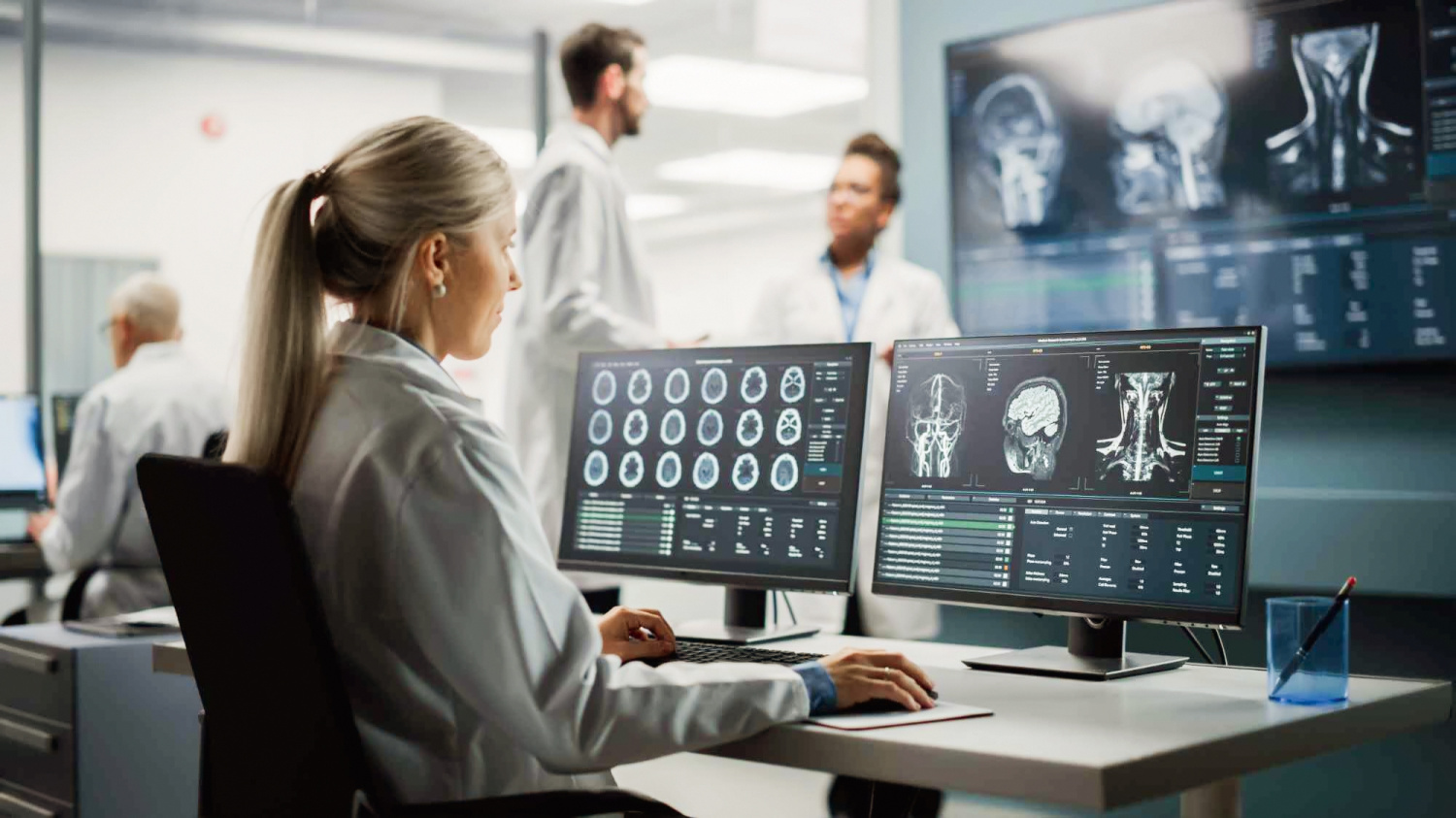
Искусственный интеллект в мировом здравоохранении. От начала до наших дней
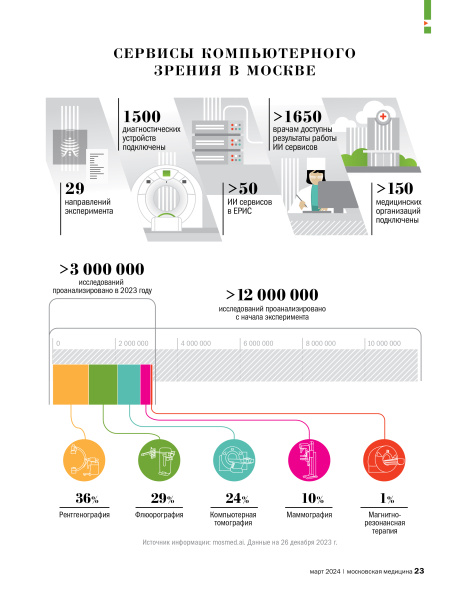
Слово «нейросеть» признано словом 2023 года по версии Института русского языка и справочно-информационного портала «Грамота. ру». Вторым по популярности, по оценке экспертов, стало слово «джипити» — GPT (Generative pre-trained transformer), то есть генеративный предобученный трансформер. Оба эти слова отражают тенденции и настрой общества на освоение искусственного интеллекта и его внедрение во все сферы жизни, в том числе в здравоохранение, где он уже нашел немало точек приложения.Инфографика
Все материалы разделаОбзор
Все материалы разделаИнтервью
Все материалы разделаЛучшие практики
Все материалы разделаОбращение руководителя ДЗМ
Все материалы раздела
Технологии искусственного интеллекта в здравоохранении
Технологии искусственного интеллекта, стремительно развиваясь, охватывают все новые сферы нашей жизни, в том числе здравоохранение, меняют подходы к превентивной медицине, диагностике и лечению заболеваний. Сегодня, например, нам стали доступны массовые скрининги на онкологические заболевания, что ранее было невозможно из-за высокой трудозатратности. Искусственный интеллект позволяет освободить наших врачей от рутинной работы, экономит их время на приеме. Обученные на достоверных данных ИИ-сервисы помогают докторам в сборе анамнеза, в назначении терапии при помощи системы поддержки принятия врачебных решений. Взятый сегодня курс на развитие персонализированного лечения также невозможен без использования технологий искусственного интеллекта. Ему поручают с помощью носимых диагностических приборов следить за состоянием здоровья хронически больных пациентов, применяется он и в разработке и клинических испытаниях новых лекарственных препаратов.
Каждый день приносит нам сообщения о новых навыках и умениях, освоенных искусственным интеллектом. Нейросети могут трудиться и день и ночь, не зная усталости, они способны в считаные минуты перебрать в базе данных сотни тысяч файлов, а найдя нужную информацию, в секунды решить сложнейшие вычислительные задачи, распознать самые мелкие детали на рентгеновских снимках и КТ-изображениях, расшифровать кардиограммы.
Все эти достижения стали достоянием московского здравоохранения. И сегодня медики столицы, занимая лидирующие позиции по внедрению технологий искусственного интеллекта в систему здравоохранения, открывают для коллег из регионов доступ к специальной платформе с сервисами искусственного интеллекта, охотно делясь опытом и наработками.
Пользуясь случаем, хотел бы поздравить коллектив журнала «Московская медицина» с 10-летним юбилеем. Темы публикаций и проблемы, которые поднимает издание, всегда
актуальны и отвечают вызовам времени. И этот номер не стал исключением.
Редакция журнала
Регистрационный номер ПИ № ФС 77-57984.
Журнал зарегистрирован Федеральной службой по надзору в сфере связи и массовых коммуникаций 28 апреля 2014 года.
Учредитель: Департамент здравоохранения города Москвы.
Издатель: НИИ организации здравоохранения и медицинского менеджмента Департамента здравоохранения города Москвы.
Адрес редакции и издателя: 115088, г. Москва, ул. Шарикоподшипниковская, 9.
Контакты: +7 (495) 530-12-89, niiozmm@zdrav.mos.ru.
Представителем авторов публикаций в журнале «Московская медицина» является издатель. Перепечатка только с согласия авторов (издателя). Мнение редакции может не совпадать c мнением автора.
Журнал представлен в РИНЦ (Российский индекс научного цитирования).
Научный редактор: Наталья Николаевна Камынина.
Редакторы: Алина Дмитриевна Хараз, Наталья Николаевна Верзилина.
Корректор: Ирина Давидовна Баринская.
Дизайнер: Ирина Львовна Тарнавская.
Сетевое издание журнал «Московская медицина» зарегистрировано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор), регистрационный номер и дата принятия решения о регистрации: серия ЭЛ № ФС 77 – 84722 от 6 февраля 2023 г.